文章来源于研发客研究院 ,作者殷丹妮 研发客(2022年11月18日)
胰高血糖素样肽-1受体(GLP-1R)激动剂正成为肥胖症的主流开发方向,且减重数据伴随着迭代产品的出现被不断刷新。
先有诺和诺德开发的司美格鲁肽击败同类产品利拉鲁肽,成为新一代减肥创新药,后有礼来的GLP-1R/GIPR双靶点激动剂替尔泊肽达到体重降幅22.5%的疗效,超过司美格鲁肽创下的减重历史。
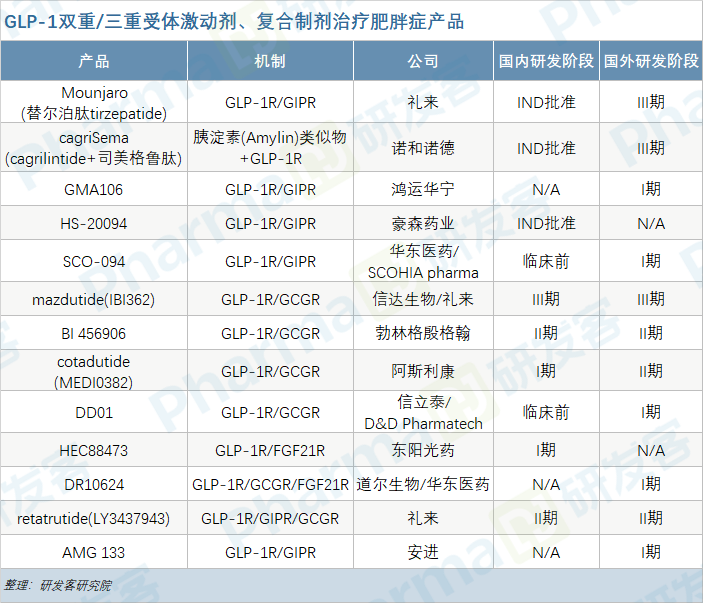
双靶点的协同作用似乎能带来更优的减重效果。国内公司有信达生物宣布其GLP-1R/GCGR双激动剂mazdutide(IBI362)获得了积极的II期数据。不仅如此,诺和诺德联合胰淀素和GLP-1开发的复方制剂cagriSema在II期临床中达到有效的减肥疗效。
GLP-1领跑的减肥赛道,已从单靶点拓展到双重、三重受体激动剂,从联合GLP-1的复合制剂延伸至胰淀素、GDF15、酪酪肽等潜在创新通路。
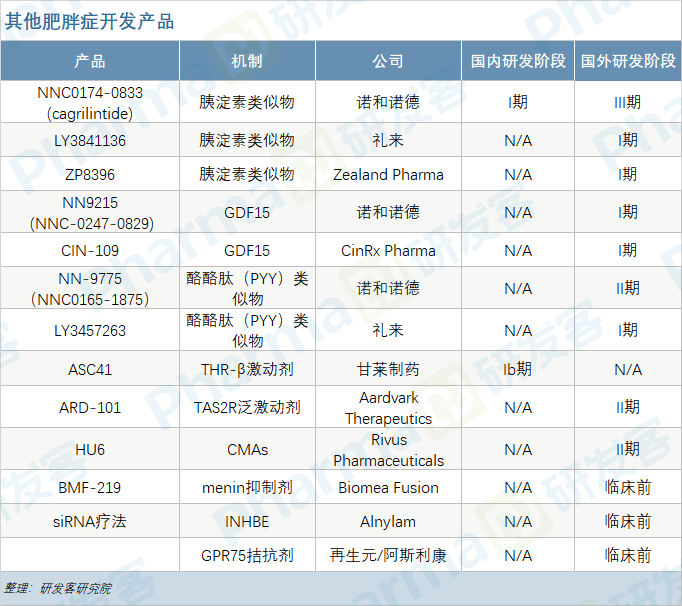
目前全球获批治疗肥胖症的GLP-1R激动剂有Saxenda(利拉鲁肽)和Wegovy(司美格鲁肽),分别于2014年和2021年获得FDA批准,均为诺和诺德开发。国内研发进展最快的是仁会生物的贝那鲁肽(HYBR-014),于2022年3月递交肥胖适应症的上市申请。GLP-1R成为减肥适应症的热门靶点,主要归因于GLP-1本身的机制特点,以及利拉鲁肽和司美格鲁肽显示出的减重疗效。研究显示,GLP-1R激动剂不仅可以促进胰岛素分泌,发挥降糖作用,还可有效延缓胃排空、降低肠道运动性,激活下丘脑的神经通路和食欲调节区域,使食欲下降、减少食物摄入,从而治疗肥胖。诺和诺德的III期临床试验数据显示,利拉鲁肽3.0mg在56周治疗期后,约62%的肥胖患者体重下降5%,34%的患者体重下降10%。这一数据支持产品在2014年上市,成为首个获批的GLP-1减肥药。此外,利拉鲁肽还在2020年将年龄扩大到12岁及以上青少年肥胖患者。56周治疗期后,利拉鲁肽组的BMI标准差评分(BMI SDS)平均降低了0.23,安慰剂组无变化。司美格鲁肽是诺和诺德开发又一款GLP-1产品,减重效果优于利拉鲁肽。在STEP 1、3、4、5和8的五项试验中,接受司美格鲁肽2.4mg治疗的肥胖症患者在68周内的平均体重减少16.9%~18.2%,2年治疗期维持在16.7%的减重水平,对比利拉鲁肽6.6%的体重降幅,司美格鲁肽能将患者体重减轻17.1%。两款GLP-1产品优异的减重效果给诺和诺德带来不俗的销售业绩,2022年前三季度共贡献113.76亿丹麦克朗(约人民币111.3亿元)的销售额,同比增长91%。显著的减重疗效和可观的经济收益也吸引国内企业竞相入局GLP-1领域。除已申请上市的仁会生物,甘李药业的GZR18、石药集团的TG103、恒瑞医药的诺利糖肽以及鸿运华宁的GMA105均分别进展至II期临床阶段。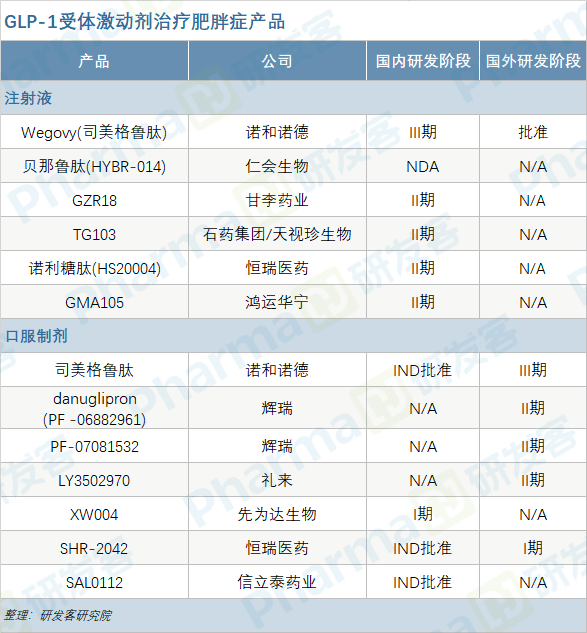 仿制药方面,国内有5家企业开发利拉鲁肽生物类似药的肥胖适应症,华东医药进度最快,其产品于今年7月已申报上市,复星医药子公司江苏万邦推进到III期临床阶段,先为达生物的ecnoglutide(XW003)进展至II期临床,此外还有九源基因、诺博特生物。尚未有企业布局司美格鲁肽生物类似药的肥胖症开发。虽然利拉鲁肽在国内并未获批用于减肥,但在广东省药学会发布的《超说明书用药目录(2020年版)》中,已将利拉鲁肽纳入超重/肥胖的超说明书使用范畴。减肥赛道的激烈竞争也吸引企业另辟口服剂型,以期获得头部优势。例如先为达生物开发的XW004是ecnoglutide的口服制剂,正处在I期临床,恒瑞医药的SHR-2042和信立泰药业的SAL0112均为口服GLP-1类似物,已获得国家药监局的临床批准。国外公司方面,诺和诺德开发的司美格鲁肽口服剂型正处于IIIa期临床阶段,预计2023年上半年结束试验。辉瑞的两款口服小分子GLP-1R激动剂danuglipron(PF-06882961)和PF-07081532都处于II期临床,礼来也布局了一款LY3502970,正在开展针对肥胖的II期研究。尚未观察到口服GLP-1RA在肥胖症中的有效数据公布。在单GLP-1RA基础上开发迭代产品,已成为国内外公司的热门竞争方向,例如双重激动剂或复合制剂,能够发挥多靶点的协同作用,优化减肥效果,同时降低副作用。礼来在双重受体激动剂开发中处于领衔优势,GLP-1R/GIPR双激动剂替尔泊肽在SURMOUNT-1的III期试验结果中展现了超过司美格鲁肽的显著减重疗效。具体而言,使用72周替西帕肽后,5mg、10mg和15mg剂量组的受试者平均减重比例分别达到16%,21.4%和22.5%。国内公司方面,信达生物从礼来引进的GLP-1R/GCGR双激动剂mazdutide(IBI362)进展速度最快,近期启动了III期GLORY-1临床研究。此前mazdutide已在低剂量组获得了积极的II期数据,在3mg、4.5mg和6mg剂量中达到主要终点,受试者的体重降幅分别达到7.21%、10.56%和11.57%,高剂量9mg、10mg的II期临床还在进行中。除信达生物外,其他公司开发的GLP-1R双激动剂都在早期阶段,且大多选择2型糖尿病作为首个开发适应症,只有较少的公司拓展至肥胖症。GLP-1R/GIPR激动剂有鸿运华宁的GMA106在澳大利亚开展I期临床,豪森药业的HS-20094获得临床IND批准。此外,还有东阳光药的GLP-1R/FGF21双靶点激动剂,以及道尔生物首创性开发的GLP-1R/GCGR/FGF21R三靶点激动剂DR10624,正在开展治疗肥胖的I期临床研究。瑞穗银行分析师预计礼来的替尔泊肽销售额在2030年将超过140亿美元。手握两款重磅减肥产品的诺和诺德自不会错过双重靶点领域,事实上,诺和诺德在2015年就推出了GLP-1R双重激动剂,但因各种原因终止了多个项目的研发,包括NN-6177、NN9709、NNC0090-2746(RG-7697)以及NN9423。在双靶点领域折戟的诺和诺德,转向开发复合制剂。8月,诺和诺德宣布复方制剂cagriSema的II期临床试验取得积极结果,达到有效的降糖和减重疗效。经过32周治疗后,cagriSema组、司美格鲁肽组和cagrilintide组的体重降幅分别达到15.6%、5.1%和8.1%。CagriSema是长效胰淀素(amylin)类似物cagrilintide和司美格鲁肽的双重复合制剂,已在国内获得肥胖/超重的临床批准。不论是GLP-1的单靶点制剂,还是双重、三重激动剂以及复合制剂,都围绕GLP-1而开发。随着对肥胖信号通路研究的深入,多种潜在治疗靶点被挖掘出来,已有部分进展到临床阶段,例如胰淀素、GDF15、酪酪肽。胰淀素(amylin)能够人体饱腹感通路来降低食物摄入、抑制肥胖症状。除诺和诺德开发的与司美格鲁肽组成复合制剂的cagrilintide,礼来于2022年3月在clinicaltrials.gov登记了amylin类似物LY3841136的I期临床研究,Zealand Pharma也开发了同类产品ZP8396。生长分化因子15(GDF15)的受体是GDNF家族受体α样(GFRAL),研究发现抑制GDF15-GFRAL通路可控制食欲和体重,故而也有公司布局,但都在早期临床,例如诺和诺德开发的NN-9775(NNC0165-1875),CinRx Pharma公司的CIN-109。酪酪肽(PYY)类似物的开发中,诺和诺德和礼来各有一款产品,其中诺和诺德正将NNC0165-1875与司美格鲁肽联用在II期研究中评估减重疗效。更多针对肥胖症的潜力产品仍在开发中,例如甘莱制药开发的THR-β激动剂ASC41、Biomea Fusion公司的menin抑制剂BMF-219。信立泰通过引入阿尔法分子科技的AI技术,合作研发肥胖症创新药。诺和诺德在今年1月与EraCal Therapeutics达成合作,期望能在斑马鱼幼鱼的药物发现平台中发现控制食欲的潜在新靶点。来自于美国临床与经济评价研究所(ICER)8月公布的一份报告表示,虽然GLP-1激动剂能减重效果明显,但价格昂贵,成本效益分析不佳。该报告比较了司美格鲁肽、利拉鲁肽以及Qsymia(芬特明/托吡酯)、Contrave(安非他酮/纳曲酮)治疗肥胖症的临床有效性和价值。根据ICER分析结果,司美格鲁肽和芬特明/托吡酯的减重疗效优于利拉鲁肽和安非他酮/纳曲酮。司美格鲁肽和利拉鲁肽除了减重效果外,还能带来心血管益处,例如改善血糖和血压,且司美格鲁肽的停药率最低。从经济成本看,司美格鲁肽和利拉鲁肽目前均定价过高,司美格鲁肽的预估净价格是每年13,618美元,降至7500美元至9800美元间才具有成本效益;利拉鲁肽的年净价是11,760美元,成本效益区间是3800美元至4800美元。芬特明/托吡酯和安非他酮/纳曲酮的年净价分别是1465美元和2094美元,相比两款GLP-1便宜很多。ICER指出,司美格鲁肽比利拉鲁肽更具成本效益,疗效更高,且负担更低。可见虽然目前GLP-1价格较高,但开发减重效果更优的产品将会带来更优的成本效益。目前国内减肥药物缺乏,芬特明/托吡酯和安非他酮/纳曲酮均未在国内上市,唯一获批的减肥药只有奥利司他。而临床结果显示奥利司他有腹泻、油性便等不良反应,长期心血管风险尚不明确。根据《中国居民营养与慢性病状况报告(2020年)》的调查结果,我国有超过一半的成年居民患有超重或肥胖,6岁以下、6~17岁的儿童和青少年超重/肥胖患病率分别达到10.4%和19%,且患病率呈上升趋势,存在很大的临床需求未得到满足。GLP-1药物的开发将给肥胖症带来新的治疗机遇。
仿制药方面,国内有5家企业开发利拉鲁肽生物类似药的肥胖适应症,华东医药进度最快,其产品于今年7月已申报上市,复星医药子公司江苏万邦推进到III期临床阶段,先为达生物的ecnoglutide(XW003)进展至II期临床,此外还有九源基因、诺博特生物。尚未有企业布局司美格鲁肽生物类似药的肥胖症开发。虽然利拉鲁肽在国内并未获批用于减肥,但在广东省药学会发布的《超说明书用药目录(2020年版)》中,已将利拉鲁肽纳入超重/肥胖的超说明书使用范畴。减肥赛道的激烈竞争也吸引企业另辟口服剂型,以期获得头部优势。例如先为达生物开发的XW004是ecnoglutide的口服制剂,正处在I期临床,恒瑞医药的SHR-2042和信立泰药业的SAL0112均为口服GLP-1类似物,已获得国家药监局的临床批准。国外公司方面,诺和诺德开发的司美格鲁肽口服剂型正处于IIIa期临床阶段,预计2023年上半年结束试验。辉瑞的两款口服小分子GLP-1R激动剂danuglipron(PF-06882961)和PF-07081532都处于II期临床,礼来也布局了一款LY3502970,正在开展针对肥胖的II期研究。尚未观察到口服GLP-1RA在肥胖症中的有效数据公布。在单GLP-1RA基础上开发迭代产品,已成为国内外公司的热门竞争方向,例如双重激动剂或复合制剂,能够发挥多靶点的协同作用,优化减肥效果,同时降低副作用。礼来在双重受体激动剂开发中处于领衔优势,GLP-1R/GIPR双激动剂替尔泊肽在SURMOUNT-1的III期试验结果中展现了超过司美格鲁肽的显著减重疗效。具体而言,使用72周替西帕肽后,5mg、10mg和15mg剂量组的受试者平均减重比例分别达到16%,21.4%和22.5%。国内公司方面,信达生物从礼来引进的GLP-1R/GCGR双激动剂mazdutide(IBI362)进展速度最快,近期启动了III期GLORY-1临床研究。此前mazdutide已在低剂量组获得了积极的II期数据,在3mg、4.5mg和6mg剂量中达到主要终点,受试者的体重降幅分别达到7.21%、10.56%和11.57%,高剂量9mg、10mg的II期临床还在进行中。除信达生物外,其他公司开发的GLP-1R双激动剂都在早期阶段,且大多选择2型糖尿病作为首个开发适应症,只有较少的公司拓展至肥胖症。GLP-1R/GIPR激动剂有鸿运华宁的GMA106在澳大利亚开展I期临床,豪森药业的HS-20094获得临床IND批准。此外,还有东阳光药的GLP-1R/FGF21双靶点激动剂,以及道尔生物首创性开发的GLP-1R/GCGR/FGF21R三靶点激动剂DR10624,正在开展治疗肥胖的I期临床研究。瑞穗银行分析师预计礼来的替尔泊肽销售额在2030年将超过140亿美元。手握两款重磅减肥产品的诺和诺德自不会错过双重靶点领域,事实上,诺和诺德在2015年就推出了GLP-1R双重激动剂,但因各种原因终止了多个项目的研发,包括NN-6177、NN9709、NNC0090-2746(RG-7697)以及NN9423。在双靶点领域折戟的诺和诺德,转向开发复合制剂。8月,诺和诺德宣布复方制剂cagriSema的II期临床试验取得积极结果,达到有效的降糖和减重疗效。经过32周治疗后,cagriSema组、司美格鲁肽组和cagrilintide组的体重降幅分别达到15.6%、5.1%和8.1%。CagriSema是长效胰淀素(amylin)类似物cagrilintide和司美格鲁肽的双重复合制剂,已在国内获得肥胖/超重的临床批准。不论是GLP-1的单靶点制剂,还是双重、三重激动剂以及复合制剂,都围绕GLP-1而开发。随着对肥胖信号通路研究的深入,多种潜在治疗靶点被挖掘出来,已有部分进展到临床阶段,例如胰淀素、GDF15、酪酪肽。胰淀素(amylin)能够人体饱腹感通路来降低食物摄入、抑制肥胖症状。除诺和诺德开发的与司美格鲁肽组成复合制剂的cagrilintide,礼来于2022年3月在clinicaltrials.gov登记了amylin类似物LY3841136的I期临床研究,Zealand Pharma也开发了同类产品ZP8396。生长分化因子15(GDF15)的受体是GDNF家族受体α样(GFRAL),研究发现抑制GDF15-GFRAL通路可控制食欲和体重,故而也有公司布局,但都在早期临床,例如诺和诺德开发的NN-9775(NNC0165-1875),CinRx Pharma公司的CIN-109。酪酪肽(PYY)类似物的开发中,诺和诺德和礼来各有一款产品,其中诺和诺德正将NNC0165-1875与司美格鲁肽联用在II期研究中评估减重疗效。更多针对肥胖症的潜力产品仍在开发中,例如甘莱制药开发的THR-β激动剂ASC41、Biomea Fusion公司的menin抑制剂BMF-219。信立泰通过引入阿尔法分子科技的AI技术,合作研发肥胖症创新药。诺和诺德在今年1月与EraCal Therapeutics达成合作,期望能在斑马鱼幼鱼的药物发现平台中发现控制食欲的潜在新靶点。来自于美国临床与经济评价研究所(ICER)8月公布的一份报告表示,虽然GLP-1激动剂能减重效果明显,但价格昂贵,成本效益分析不佳。该报告比较了司美格鲁肽、利拉鲁肽以及Qsymia(芬特明/托吡酯)、Contrave(安非他酮/纳曲酮)治疗肥胖症的临床有效性和价值。根据ICER分析结果,司美格鲁肽和芬特明/托吡酯的减重疗效优于利拉鲁肽和安非他酮/纳曲酮。司美格鲁肽和利拉鲁肽除了减重效果外,还能带来心血管益处,例如改善血糖和血压,且司美格鲁肽的停药率最低。从经济成本看,司美格鲁肽和利拉鲁肽目前均定价过高,司美格鲁肽的预估净价格是每年13,618美元,降至7500美元至9800美元间才具有成本效益;利拉鲁肽的年净价是11,760美元,成本效益区间是3800美元至4800美元。芬特明/托吡酯和安非他酮/纳曲酮的年净价分别是1465美元和2094美元,相比两款GLP-1便宜很多。ICER指出,司美格鲁肽比利拉鲁肽更具成本效益,疗效更高,且负担更低。可见虽然目前GLP-1价格较高,但开发减重效果更优的产品将会带来更优的成本效益。目前国内减肥药物缺乏,芬特明/托吡酯和安非他酮/纳曲酮均未在国内上市,唯一获批的减肥药只有奥利司他。而临床结果显示奥利司他有腹泻、油性便等不良反应,长期心血管风险尚不明确。根据《中国居民营养与慢性病状况报告(2020年)》的调查结果,我国有超过一半的成年居民患有超重或肥胖,6岁以下、6~17岁的儿童和青少年超重/肥胖患病率分别达到10.4%和19%,且患病率呈上升趋势,存在很大的临床需求未得到满足。GLP-1药物的开发将给肥胖症带来新的治疗机遇。